Importância
Ostertagia ostertagi é um nematóide gastrointestinal de bovinos considerado um dos parasitas de maior impacto econômico na bovinocultura de leite e corte em regiões de clima temperado e subtropical. Parasita exclusivo do abomaso, atua de forma insidiosa: mesmo em infecções subclínicas — sem sinais clínicos evidentes — provoca queda significativa na conversão alimentar, redução da produção leiteira, retardo no crescimento de animais jovens e prejuízos reprodutivos.
No Brasil, sua relevância é mais expressiva nas regiões Sul e Sudeste, onde o clima favorece o desenvolvimento larval nas pastagens. Frequentemente subestimado por sua apresentação subclínica predominante, O. ostertagi é responsável por perdas silenciosas nos rebanhos, muitas vezes não associadas ao parasitismo sem investigação diagnóstica adequada. Em escala mundial, é considerado o nematóide gastrintestinal de bovinos com maior impacto econômico global, superando até mesmo Haemonchus em sistemas de produção leiteira intensiva.
História e Descoberta
- Descobridor: Stiles & Henry, pesquisadores norte-americanos, descreveram formalmente Ostertagia ostertagi em 1913, embora o gênero Ostertagia já tivesse sido proposto por Ransom em 1907 para agrupar nematóides abomasais morfologicamente semelhantes.
O reconhecimento de Ostertagia ostertagi como agente de doença bovina se consolidou gradualmente ao longo do século XX. Ainda na primeira metade do século, surtos de diarreia profusa e emaciação em bovinos jovens na Europa — especialmente no Reino Unido, Irlanda e Países Baixos — foram associados a infecções maciças por esse parasita, quadro que passou a ser denominado “ostertagiose”. A relevância clínica do parasita, no entanto, só foi plenamente compreendida quando estudos nas décadas de 1950 e 1960 demonstraram que as larvas de quarto estágio (L4) podiam entrar em hipobiose — um estado de desenvolvimento arrestado — nas glândulas gástricas do hospedeiro, permanecendo inativas por meses antes de retomar o desenvolvimento. Esse fenômeno, denominado ostertagiose Tipo II, explicava surtos de doença em pleno inverno, muito tempo após o fim da estação de pastejo contaminado, e revolucionou a compreensão do controle estratégico da parasitose. No Brasil, estudos epidemiológicos nas décadas de 1980 e 1990 documentaram a presença e relevância de O. ostertagi principalmente em bovinos leiteiros no Sul e Sudeste do país, consolidando a necessidade de incluí-lo nos programas de controle parasitário regional.
Classificação Taxonômica de Ostertagia ostertagi
- Reino: Animalia
- Filo: Nematoda
- Classe: Chromadorea
- Ordem: Rhabditida
- Família: Trichostrongylidae
- Gênero: Ostertagia
- Espécie: O. ostertagi
Morfologia
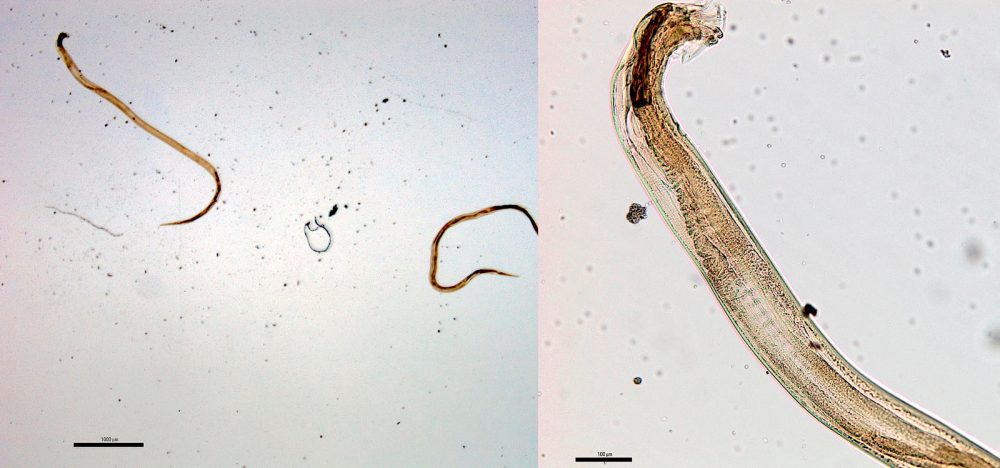
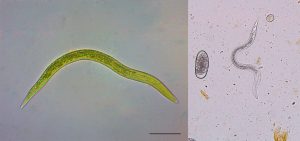
Ostertagia ostertagi é um nematóide de pequeno a médio porte, com coloração acastanhada — característica que rendeu ao grupo o apelido de “vermes marrons do estômago” (brown stomach worms). Os machos medem entre 6 e 9 mm de comprimento, enquanto as fêmeas são ligeiramente maiores, atingindo 8 a 12 mm. O corpo é filiforme e delgado, com cutícula finamente estriada transversalmente.
A extremidade anterior apresenta cápsula bucal pequena e rudimentar, adaptada para a alimentação nas células das glândulas gástricas, e não para hematofagia ativa como em Haemonchus. O macho possui bolsa copulatória bem desenvolvida, com espículos longos e bifurcados na extremidade, característica importante para a diferenciação de espécies do complexo Ostertagia. A fêmea apresenta vulva com rebordo cuticular proeminente (sobrelevação vulvar), útil para identificação à necropsia. Os ovos são típicos de tricostrongilídeos: elipsoides, de casca fina e com mórula em estágio inicial de segmentação no momento da eliminação pelas fezes, medindo aproximadamente 70–85 µm de comprimento por 35–45 µm de largura — morfologicamente semelhantes aos de outros tricostrongilídeos, tornando a diferenciação por ovos praticamente impossível sem coproculturas ou métodos moleculares.
Epidemiologia de Ostertagia ostertagi
Ostertagia ostertagi tem distribuição cosmopolita, com maior prevalência em regiões de clima temperado e subtropical úmido. No Brasil, concentra-se principalmente nos estados do Rio Grande do Sul, Santa Catarina, Paraná e nas regiões serranas de São Paulo e Minas Gerais. A espécie é adaptada a temperaturas amenas e alta umidade, sendo a sobrevivência das larvas no ambiente inversamente proporcional ao calor e à seca — condições que limitam sua relevância nas regiões Nordeste e Centro-Oeste brasileiras.
O ciclo de vida é direto, sem hospedeiro intermediário. Os ovos eliminados pelas fezes eclodem no ambiente, desenvolvendo-se em larvas L1, L2 e L3 infectantes na pastagem. As L3 são envoltas por uma bainha protetora que aumenta sua resistência ambiental; em condições favoráveis, podem sobreviver na pastagem por meses. A infecção ocorre pela ingestão de L3 durante o pastejo. No abomaso, as larvas penetram nas glândulas gástricas (glândulas de Lieberkühn do abomaso), onde se desenvolvem até L4 e, posteriormente, para adultos.
Um aspecto epidemiológico fundamental é a hipobiose larval: em resposta a estímulos sazonais — principalmente fotoperíodo reduzido e queda de temperatura no outono/inverno do hemisfério sul — as larvas L4 entram em estado de desenvolvimento arrestado dentro das glândulas gástricas. Esse fenômeno é responsável pela ostertagiose Tipo II, que ocorre no final do inverno ou início da primavera, quando as larvas em hipobiose retomam o desenvolvimento sincronizadamente, liberando milhares de adultos jovens de forma abrupta. Os principais fatores de risco incluem: bovinos jovens entre 6 e 18 meses, pastagens contaminadas em períodos úmidos, ausência de vermifugação estratégica e sistemas de produção com alta densidade animal.
Patogenia
A ação patogênica de Ostertagia ostertagi é exercida principalmente pelas larvas L4 e pelos adultos jovens nas glândulas gástricas do abomaso. A penetração e o desenvolvimento larval nas glândulas provocam destruição das células parietais produtoras de ácido clorídrico, com substituição das células especializadas por células indiferenciadas de tipo fetal — processo denominado transformação foveolar. Essa lesão resulta em hipocloridria (redução da acidez gástrica), com elevação do pH abomasal de valores normais em torno de 2–3 para valores próximos a 7.
A hipocloridria tem consequências em cascata: compromete a ativação do pepsinogênio em pepsina, prejudicando a digestão proteica; permite a proliferação bacteriana no abomaso; e leva à elevação plasmática do pepsinogênio — importante marcador diagnóstico da ostertagiose. A hipoalbuminemia resultante da má digestão e da perda proteica para o lúmen abomasal provoca edema submandibular (“queixo d’água”), ascite e diarreia osmótica. Nas infecções maciças características da ostertagiose Tipo II, a emergência sincronizada de milhares de larvas em hipobiose causa ruptura extensa das glândulas gástricas, com resposta inflamatória aguda intensa, edema de mucosa abomasal e deterioração clínica rápida.
Sinais Clínicos
Ostertagiose Tipo I (animais jovens, fase patente): Ocorre principalmente em bovinos entre 6 e 18 meses durante o primeiro verão/outono em pastagem contaminada. Os sinais incluem diarreia aquosa persistente (às vezes profusa, de coloração esverdeada), perda de peso progressiva, pelagem opaca e sem brilho, redução do apetite e queda no ganho de peso. Em casos graves, observam-se edema submandibular, fraqueza e prostração. A mortalidade pode ocorrer em animais com cargas parasitárias muito elevadas e sem tratamento.
Ostertagiose Tipo II (animais adultos, emergência de hipobiose): Ocorre no final do inverno ou início da primavera, frequentemente em bovinos adultos — inclusive vacas em lactação. O quadro é mais agudo e grave que o Tipo I, com diarreia intensa, hipoproteinemia acentuada, edema submandibular marcado (“bottlejaw”), perda de peso rápida e queda abrupta na produção leiteira. A mortalidade é mais elevada nessa forma e pode surpreender produtores que não associam o quadro ao parasitismo, pois ocorre fora da estação de pastejo ativo.
Forma subclínica (qualquer faixa etária): Frequentemente a mais relevante do ponto de vista econômico. Sem sinais clínicos evidentes, mas com redução mensurável no ganho de peso diário (até 15–20%), queda na produção leiteira, piora da conversão alimentar e comprometimento da função reprodutiva. Essa forma só é detectada por monitoramento laboratorial ou por avaliação do desempenho zootécnico do rebanho.
Diagnóstico
- Métodos Tradicionais: A contagem de ovos por grama de fezes (OPG) pela técnica de McMaster é o método de triagem mais utilizado, mas apresenta limitação importante: na ostertagiose Tipo II, as larvas em hipobiose não produzem ovos, resultando em OPG próximo de zero mesmo em infecções maciças. A coprocultura com identificação larval de terceiro estágio (L3) permite diferenciar O. ostertagi de outros tricostrongilídeos, embora seja trabalhosa. A dosagem de pepsinogênio sérico é um marcador bioquímico sensível da disfunção abomasal — valores elevados (acima de 3 unidades de tirosina) são fortemente sugestivos de ostertagiose, especialmente na Tipo II. À necropsia, a mucosa abomasal apresenta aspecto característico em “marrocos” (superfície nodular com múltiplos nódulos umbilicados), patognomônico da lesão por Ostertagia.
- Métodos Moleculares/Sorológicos: A PCR em tempo real (qPCR) aplicada a amostras de fezes permite a detecção e quantificação específica de O. ostertagi, com vantagem especial na fase de hipobiose, quando o OPG é negativo. Testes de ELISA para detecção de anticorpos séricos ou em leite têm sido desenvolvidos e validados para uso em rebanhos leiteiros, permitindo monitoramento não invasivo da exposição ao parasita em nível de rebanho — ferramenta especialmente útil para bovinos em lactação.
- Indicação de Teste: A investigação de O. ostertagi é recomendada em bovinos jovens com diarreia persistente e baixo desempenho zootécnico, em bovinos adultos com quadro de hipoproteinemia e queda de produção leiteira no final do inverno, e em rebanhos com desempenho abaixo do esperado sem causa identificada. O monitoramento periódico de pepsinogênio sérico e ELISA de leite em rebanhos leiteiros de regiões de risco é uma estratégia de vigilância eficiente e custo-efetiva.
Tratamento
O tratamento da ostertagiose bovina requer atenção ao estágio da parasitose, pois nem todos os fármacos são igualmente eficazes contra larvas em hipobiose:
- Benzimidazóis (fenbendazol, albendazol, oxfendazol): apresentam boa eficácia contra adultos e larvas L4 em desenvolvimento ativo. O fenbendazol em doses múltiplas ou prolongadas demonstra eficácia razoável contra larvas em hipobiose, sendo frequentemente indicado na ostertagiose Tipo II.
- Lactonas macrocíclicas (ivermectina, doramectina, abamectina, eprinomectina): altamente eficazes contra adultos e larvas L4 ativas; a eficácia contra larvas em hipobiose é variável conforme o produto e a formulação. A eprinomectina possui vantagem adicional por não apresentar período de carência para o leite, sendo a opção preferencial em vacas em lactação.
- Levamisol: boa eficácia contra adultos e L4 ativas, mas eficácia limitada contra larvas em hipobiose; não recomendado como monoterapia para ostertagiose Tipo II.
Em rebanhos com suspeita de resistência anti-helmíntica, recomenda-se a realização do teste de redução de contagem de ovos nas fezes (FECRT) para avaliar a eficácia dos produtos disponíveis antes de definir o protocolo de tratamento.
Prevenção e Controle
Medidas sanitárias: O manejo de pastagens é fundamental: a rotação de piquetes com períodos de descanso adequados reduz a densidade de larvas infectantes disponíveis. Em regiões de risco, a retirada de animais jovens das pastagens mais contaminadas durante os meses de maior risco (outono) pode ser estratégica. A adubação nitrogenada das pastagens, embora benéfica para a produção forrageira, pode aumentar a sobrevivência larval ao reduzir a dessecação do solo.
Manejo de hospedeiros: A vermifugação estratégica, baseada no monitoramento epidemiológico regional, é a principal ferramenta de controle. Em regiões do Sul do Brasil, recomenda-se vermifugação no outono — antes do período de hipobiose — para reduzir o acúmulo de larvas nas glândulas gástricas, e no final do inverno/início da primavera — antes da emergência das larvas em hipobiose — para prevenir a ostertagiose Tipo II. O monitoramento regular de OPG e pepsinogênio sérico permite ajustar os protocolos de vermifugação conforme a real situação parasitária do rebanho, evitando tratamentos desnecessários e reduzindo a pressão de seleção para resistência. A integração com o diagnóstico molecular por PCR é especialmente recomendada em rebanhos leiteiros de alta produção.
Estudos Recentes
As pesquisas mais recentes sobre Ostertagia ostertagi têm avançado em duas frentes de destaque. A primeira é o desenvolvimento e validação de ferramentas de diagnóstico indireto para uso em rebanhos leiteiros, especialmente testes de ELISA aplicados ao leite de tanque — que permitem estimar o nível de exposição ao parasita em todo o rebanho a partir de uma única amostra, sem a necessidade de coleta individual de fezes ou sangue. Esses testes têm sido incorporados em programas de monitoramento de saúde de rebanho em países europeus e avaliados para adaptação ao contexto brasileiro.
A segunda frente envolve estudos sobre resistência anti-helmíntica. Relatos de populações de O. ostertagi com redução de sensibilidade a benzimidazóis e lactonas macrocíclicas têm aumentado em rebanhos europeus e norte-americanos com histórico de tratamentos frequentes e não monitorados. A caracterização molecular dos mecanismos de resistência — especialmente mutações no gene da beta-tubulina para benzimidazóis — e o desenvolvimento de marcadores genéticos para seu monitoramento em campo representam uma área ativa de investigação com implicações diretas para as estratégias de controle no Brasil.
Curiosidades
- Fato Interessante: Ostertagia ostertagi é capaz de detectar sinais ambientais do hospedeiro — como variações no fotoperíodo e temperatura — e “programar” suas larvas L4 para entrar em hipobiose ainda dentro do animal. Esse estado de desenvolvimento suspense pode durar até cinco meses, período em que as larvas permanecem metabolicamente quase inativas nas glândulas gástricas, invisíveis ao diagnóstico convencional por OPG e resistentes à maioria dos anti-helmínticos — uma estratégia evolutiva que garante a sobrevivência do parasita durante os meses de inverno, quando não há larvas infectantes nas pastagens.
Referências
- OIE/WOAH – Bovine Ostertagiosis
- CFSPH Iowa State University – Ostertagiosis
- FAO – Worm Control for Small Ruminants in Tropical Asia